세계 최초 실험실 배양 식도가 돼지에서 작동했다 — 장기 의학의 판이 바뀔 수 있다
한줄 요약
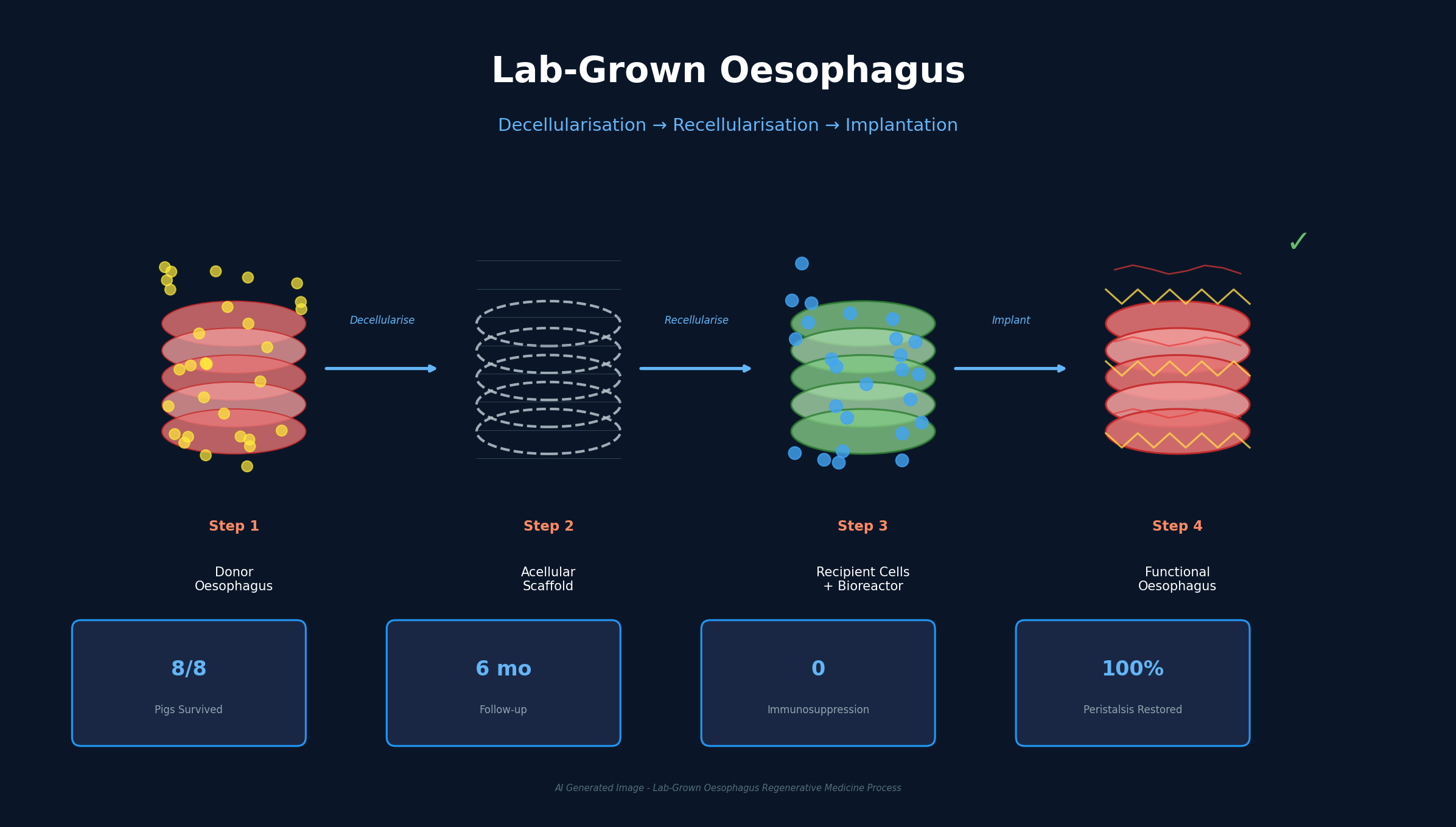
돼지 기증 장기에서 세포를 벗겨내고 수혜자의 세포를 심어 만든 식도가 면역억제제 없이 6개월간 정상 기능을 유지했다. 선천성 식도폐쇄증으로 태어나는 아이들에게 근본적 치료의 가능성이 열리고 있다.
핵심 포인트
탈세포화-재세포화 접근법의 세계 최초 완전 구현
UCL과 GOSH 연구진이 기증자 돼지의 식도에서 모든 세포를 화학적으로 제거하여 자연 스캐폴드를 만들고, 수혜자 돼지의 근육세포를 채취해 실험실에서 대량 증식시킨 뒤 스캐폴드에 주입했다. 바이오리액터에서 1주일간 성장 용액을 순환시키는 과정을 포함해 전체 제작에 약 2개월이 소요된다. 이전 연구들이 부분적 성공을 거뒀지만, 탈세포화부터 이식, 기능 회복까지 전체 파이프라인을 하나로 완성한 것은 이번이 세계 최초다.
면역억제제 없이 6개월간 완전한 기능 회복 달성
이식된 식도는 면역억제제를 전혀 사용하지 않고도 8마리 돼지 전원이 첫 달을 생존했으며, 6개월 후에는 근육층, 신경, 혈관이 모두 재생되었다. 식도의 연동운동(peristalsis)이 완전히 회복되어 음식을 정상적으로 위로 밀어 넣는 기능이 확인되었다. 기존 장기 이식에서 면역억제제는 평생 복용이 필수이며 감염 취약성과 암 발생률 2~4배 증가라는 부작용을 수반하는데, 이 방법은 그 필요성을 원천적으로 제거한다.
성장하는 동물 모델에서의 성공이 소아 적용 가능성 입증
실험이 빠르게 성장하는 어린 돼지에서 이루어졌다는 점은 임상적으로 매우 중요하다. 어린 돼지는 체내 장기도 함께 커져야 하며, 이식된 식도가 이 성장에 적응했다는 것은 빠르게 자라는 소아 환자에게 적용될 수 있는 강력한 근거가 된다. 식도폐쇄증은 출생 10,000명당 2.3~2.6명에게 발생하는 선천성 기형으로, 현재 치료법으로는 위나 대장 조직을 떼어 식도를 대체하는 복잡한 재건술에 의존하고 있다.
관형 장기 전반으로 확장 가능한 플랫폼 기술
탈세포화-재세포화 접근법은 식도에만 국한되지 않는다. 기관(trachea), 소장, 방광, 혈관 등 관형(tubular) 장기 전반에 적용 가능한 기반 기술이다. UCL-GOSH 팀의 Paolo De Coppi 교수도 다른 질환 분야로의 번역 가능성을 열어준다고 밝혔다. 전 세계적으로 10만 명 이상이 장기 이식 대기 명단에 올라 있으며 미국에서만 매일 17명이 장기를 기다리다 사망하는 현실에서, 이 플랫폼 기술의 잠재적 파급력은 식도 하나에 국한되지 않는다.
조직공학 시장 431억 달러 성장세와 상업화 가능성
2024년 약 193억 달러 규모였던 조직공학 시장은 2030년까지 431억 달러로 성장할 전망이며 연평균 성장률 14.3%에 달한다. 바이오재료, 3D 바이오프린팅, 줄기세포 연구, 유전자 편집 기술의 동시다발적 발전이 시장을 견인하고 있다. 아시아 태평양 지역은 연 19% 이상의 가장 빠른 성장률을 보일 전망이다. UCL-GOSH의 이번 성과는 학술적 돌파를 넘어 상업화 가능성을 입증한 사례로, Organogenesis, United Therapeutics 등 바이오텍 기업들의 투자와 관심을 끌어모을 것이다.
긍정·부정 분석
긍정적 측면
- 선천성 식도폐쇄증 아이들에게 건강한 장기를 희생하지 않는 근본적 치료 제공
현재 long-gap 식도폐쇄증 치료는 위나 대장 조직을 떼어 식도를 대체하는 복잡한 재건술에 의존하며, 건강한 장기를 손상시키는 대가를 치른다. 실험실 배양 식도가 임상에 도입되면 이런 희생 없이 온전한 식도를 제공할 수 있다. 8마리 돼지 전원 생존과 6개월간 정상 삼킴 기능 회복은 안전성과 유효성을 동시에 입증한다.
- 면역억제제 불필요로 소아 환자의 삶의 질 혁신적 개선
현재 장기 이식 환자들은 평생 면역억제제를 복용하며 감염 취약성과 암 발생률 2~4배 증가 위험을 감수한다. 소아 환자는 수십 년간 이 약을 복용해야 한다. 탈세포화-재세포화 방식은 아이의 자기 세포로 만든 장기이므로 면역 시스템이 공격할 이유가 없어 이 부담을 근본적으로 제거한다.
- 연 14.3% 성장하는 조직공학 시장이 상업화를 견인
2024년 193억 달러에서 2030년 431억 달러로 성장 전망인 조직공학 시장은 바이오재료, 3D 바이오프린팅, 줄기세포 연구의 동시 발전으로 강력한 성장세를 보인다. 아시아 태평양 지역은 19% 이상의 가장 빠른 성장률을 기록할 전망이다. 이번 연구는 학술적 돌파를 넘어 상업화 가능성을 입증했다.
- 관형 장기 전반으로 확장 가능한 플랫폼 기술의 잠재력
식도 성공은 기관, 소장, 방광, 혈관 등 관형 장기 전반에 적용 가능한 기반 기술이 검증되었음을 의미한다. 한 번의 성공이 여러 질환 영역으로 파급될 수 있어 연구 가치가 식도폐쇄증 하나보다 훨씬 크다. 장기 기증자 부족으로 매년 수천 명이 대기 명단에서 사망하는 현실을 바꿀 잠재력이 있다.
- Nature Biotechnology 발표로 학술적 신뢰성 검증
세계 최고 수준의 동료심사 저널에 발표된 만큼 연구 방법론과 결과의 신뢰성이 검증되었다. GOSH 자선재단과 영국 MRC의 지원을 받은 연구로 지속적인 후속 연구 기반이 마련되어 있다. 전 세계 재생의학 연구 그룹들의 독립적 재현 시도가 이어질 것이다.
우려되는 측면
- 동물 모델 성공이 인간 임상으로 직결되지 않을 위험
돼지 식도가 인간과 해부학적으로 유사하지만 면역 반응의 미묘한 차이, 인간 세포의 증식 특성, 장기간 합병증 가능성은 실제 인간 임상시험에서만 확인 가능하다. 의학 역사에는 동물 실험에서 극적으로 성공하고도 인간 임상에서 좌절한 사례가 수없이 많다. 유전자 치료에서 인공 심장까지 선례가 풍부하다.
- 2개월 제작 기간이 응급 신생아 치료에 부적합
식도폐쇄증은 출생 직후 진단되는 응급 상황으로 아기는 식도 없이 오래 버틸 수 없다. 2개월이라는 제작 기간은 이 응급성과 양립하기 어렵다. 산전 진단으로 미리 준비하거나 기존 수술 후 2차 수술로 이식하는 전략이 필요하며, 이는 추가적인 규제 승인과 임상 프로토콜 변경을 요구한다.
- 초기 고비용과 선진국 편중으로 의료 불평등 심화 우려
세포 채취, 배양, 바이오리액터 운영, 품질 관리, 이식 수술까지 고비용 과정이 수반된다. 초기에는 영국, 미국, 일본 등 선진국 대형 의료기관에서만 가능할 것이며, 기술이 가장 절실한 개발도상국 환자들은 오랜 기간 소외될 수 있다. 시장 성장이 접근성의 민주화를 의미하지는 않는다.
- 규제 프레임워크 미확립으로 승인까지 10년 이상 소요 전망
실험실 배양 장기는 의약품도 의료기기도 아닌 새로운 범주의 치료제로 FDA, EMA 등이 명확한 승인 프레임워크를 아직 완전히 확립하지 못했다. 세포치료제와 조직공학 제품의 규제 경로는 기존 의약품보다 훨씬 복잡하고 시간이 오래 걸린다. 첫 인간 임상시험까지 3~5년, 규제 승인까지 10년 이상이 현실적 전망이다.
- 6개월 추적으로는 수십 년 단위의 내구성 보장 불가
6개월은 기능 회복 확인에 의미 있지만 수십 년 단위 내구성을 보장하기엔 턱없이 짧다. 이식된 식도가 10~20년 후에도 정상 기능하는지, 예상치 못한 조직 변성이나 종양 발생 위험은 없는지 아직 아무도 답할 수 없다. 소아 환자는 성장과 노화 과정을 모두 거쳐야 하므로 장기 안전성이 더욱 중요하다.
전망
단기적으로, 향후 1~6개월 사이에 이 연구의 가장 직접적인 파급은 학계와 바이오텍 업계의 관심 폭발이 될 것이다. Nature Biotechnology에 발표된 만큼, 전 세계 재생의학 연구 그룹들이 이 프로토콜을 자체적으로 검증하고 재현하려는 시도가 이어질 것이다. UCL-GOSH 팀은 이미 영국 의학연구위원회(MRC)와 GOSH 자선재단의 지원을 받고 있으며, 이번 성과를 기반으로 추가 연구 기금을 확보하는 것은 시간문제다. 바이오텍 기업 측면에서는 이 기술의 라이선싱이나 공동 개발 제안이 쏟아질 가능성이 높다. 재생의학 분야의 대표적 기업인 Organogenesis, United Therapeutics, Miromatrix Medical 등이 관형 장기 조직공학에 대한 투자를 확대할 것으로 예상한다. 특히 United Therapeutics는 이미 돼지 장기를 활용한 이종이식(xenotransplantation) 분야에서 대규모 투자를 진행하고 있어, 자가 세포 기반 접근법으로의 포트폴리오 확장이 자연스럽다. 학술적으로는 이번 논문이 재생의학 분야의 리뷰 논문과 교과서에 즉각 반영될 것이며, 관련 학회에서의 초청 강연과 세미나가 급증할 것이다.
동물 모델 데이터의 보완도 이 시기에 이루어질 전망이다. 현재 8마리 돼지에서 6개월간의 추적 결과만 발표된 상태이므로, 12개월과 24개월 추적 데이터가 추가로 공개될 것이다. 이 장기 추적 결과가 긍정적이라면 인간 임상시험을 위한 규제기관 사전 상담(pre-IND meeting)이 시작될 수 있다. 영국의 MHRA(의약품 및 건강관리제품규제청)가 첫 규제 접촉 대상이 될 가능성이 가장 높으며, 미국 FDA의 생물의약품평가연구센터(CBER)도 병행 접촉이 예상된다. 또한 일본의 PMDA(의약품의료기기종합기구)도 주목할 필요가 있는데, 일본은 2014년부터 재생의학 제품에 대한 조건부 승인 제도를 세계 최초로 운영해온 나라이기 때문이다. 아시아태평양 지역의 조직공학 시장이 연 19% 이상의 성장률을 보이고 있다는 점도 일본과 한국의 규제기관이 이 기술에 일찍 관심을 가질 동기를 제공한다.
중기적으로, 6개월에서 2년 사이에는 이 기술의 임상 번역(clinical translation)을 위한 본격적인 준비가 진행될 것이다. 가장 중요한 과제는 GMP(우수의약품제조관리기준) 등급의 제조 공정을 확립하는 것이다. 연구실 수준에서 성공한 프로토콜을 임상 수준으로 격상시키려면, 세포 배양 환경의 무균 등급, 바이오리액터의 정밀 사양, 중간 공정 품질 관리 지표, 최종 제품의 출하 기준, 멸균 절차 등 모든 공정이 규제 기준에 맞게 표준화되어야 한다. 이 과정에서 제조 비용의 윤곽이 드러나게 되며, 이 기술의 경제적 실현 가능성이 본격적인 시험대에 오르게 된다. GMP 전환은 통상적으로 18개월에서 36개월이 소요되며, 이 기간 동안의 기술 이전과 공정 검증이 전체 타임라인의 병목이 될 수 있다.
나는 첫 인간 임상시험이 2028년 후반에서 2029년 사이에 시작될 것으로 전망한다. 대상은 기존 치료에 실패했거나 적합한 수술 방법이 없는 장갭 식도폐쇄증(long-gap oesophageal atresia) 환자, 특히 소아 환자가 될 것이다. 임상시험 설계는 안전성 중심의 Phase I/II 형태가 유력하며, 5명에서 10명 내외의 소규모 코호트로 시작할 것이다. 영국의 GOSH가 첫 임상시험 사이트가 될 가능성이 높고, 미국의 보스턴 어린이병원이나 필라델피아 어린이병원이 다기관 시험에 참여할 수 있다. 이 시험의 1차 평가변수(primary endpoint)는 이식 후 12개월 시점의 식도 기능과 안전성이 될 것이며, 2차 평가변수(secondary endpoint)로 삼킴 기능 점수, 영양 상태 지표, 체중 및 성장 곡선, 위식도역류 발생률, 삶의 질 평가 등이 포함될 것이다.
이 시기에 주목해야 할 또 다른 발전은 3D 바이오프린팅과의 기술 융합이다. 현재 UCL 팀의 방법은 기증자 돼지의 식도를 스캐폴드로 사용하지만, 3D 바이오프린팅 기술이 성숙하면 합성 바이오재료로 스캐폴드를 직접 제작할 수 있게 된다. 이는 동물 유래 스캐폴드에 대한 의존성을 제거하고, 개별 환자의 해부학적 특성에 맞춘 완벽한 맞춤형 장기 제작을 가능하게 한다. Aspect Biosystems와 BICO(구 CELLINK) 같은 기업들이 이미 이 방향으로 대규모 투자를 진행하고 있으며, 합성 스캐폴드와 탈세포화 스캐폴드를 결합한 하이브리드 접근법이 차세대 표준이 될 가능성도 있다. 이러한 융합 기술은 제조 시간을 2개월에서 2~3주로 단축할 잠재력을 가지고 있어, 현재의 가장 큰 임상적 제약인 긴 제작 기간 문제를 해결할 열쇠가 될 수 있다.
장기적으로, 2년에서 5년 이상의 시간 지평에서 보면, 이번 연구는 맞춤형 장기 의학(personalized organ medicine)이라는 새로운 의학 분야의 탄생을 알리는 신호탄이 될 것이다. 가장 낙관적인 시나리오(bull case)에서는 2030년대 초반까지 식도를 포함한 3종에서 5종의 관형 장기에 대해 표준화된 배양 프로토콜이 확립되고, 최소 10개국 이상에서 규제 승인을 받는다. 조직공학 시장이 2030년 431억 달러에서 2035년 1000억 달러를 돌파하며, 맞춤형 장기가 전체 시장의 15%에서 20%를 차지하게 된다. 관형 장기에 한정한 이식 대기 목록 사망률이 현재 대비 30%에서 40% 감소하는 극적인 변화가 나타날 수 있다.
기본 시나리오(base case)에서는 2030년대 중반까지 식도와 기관(trachea) 2개 장기에 대해 임상 승인이 이루어지고, 전 세계 20개에서 30개 선진 의료기관에서 시술이 가능해진다. 시술 비용은 건당 10만에서 25만 달러 수준으로 안정화되며, 기존의 복잡한 재건 수술과 비교해 초기 비용은 높지만 장기적으로는 합병증 치료비 절감과 면역억제제 비용 제거를 통해 비용 효율성이 입증된다. 보험 적용은 제한적이며, 주로 기존 치료에 실패한 환자를 대상으로 승인될 가능성이 높다. 맞춤형 장기가 조직공학 시장의 5%에서 10%를 차지하게 되고, 연간 약 500건에서 1000건의 시술이 전 세계적으로 시행된다.
비관적 시나리오(bear case)에서는 인간 임상시험에서 예상치 못한 합병증이 발생하여 개발이 지연된다. 면역 반응이 돼지와 달리 인간에서 완전히 억제되지 않거나, 이식된 조직에서 장기적으로 섬유화나 협착이 발생할 가능성이 있다. 또한 GMP 제조 공정의 표준화가 예상보다 어려워 배치(batch) 간 재현성 문제가 대두될 수도 있다. 이 경우 프로토콜의 근본적 수정이 필요해지며, 규제 승인까지 15년 이상이 걸릴 수 있고, 임상 적용은 2040년대로 밀려날 수 있다. 그래도 이 과정에서 축적된 세포 배양 데이터와 바이오리액터 기술, 탈세포화 프로토콜은 다른 재생의학 분야에 간접적으로 기여할 것이며, 특히 피부 재생, 연골 재건, 상처 치유 분야에서의 응용이 기대된다.
내가 가장 주시하는 세 가지 핵심 변수가 어떤 시나리오가 현실화될지를 결정할 것이다. 첫째, 인간 세포의 스캐폴드 내 생착률이다. 돼지 세포만큼 효율적으로 인간의 근육세포와 전구세포가 탈세포화된 스캐폴드에 부착하고 증식할 수 있는지가 핵심이다. 둘째, 장관신경계(enteric nervous system)의 신경 재생 수준이다. 식도의 연동운동은 이 신경망에 의해 제어되며, 완전한 재생이 장기적 기능 유지에 핵심적이다. 돼지에서의 6개월간 신경 재생은 고무적이나 인간에서도 동일한 수준이 달성될 것이라는 보장은 없다. 셋째, 제조 비용의 하락 속도다. 세포 배양과 바이오리액터 기술의 자동화가 얼마나 빠르게 진행되느냐에 따라, 이 기술이 소수 병원의 프리미엄 치료로 남을지 폭넓게 보급될지가 결정된다.
재생의학의 더 넓은 맥락에서, 이 연구는 장기를 고치는 의학에서 장기를 만드는 의학으로의 전환에서 결정적인 이정표가 될 것이다. 현재 전 세계적으로 10만 명 이상이 장기 이식 대기 명단에 올라 있으며, 미국에서만 매일 17명이 장기를 기다리다 사망한다. 맞춤형 배양 장기가 현실화되면 이 비극적인 통계를 근본적으로 바꿀 수 있다. 물론 심장이나 간 같은 복잡한 실질 장기의 배양은 관형 구조인 식도보다 훨씬 어려운 도전이지만, 관형 장기에서의 성공은 그 방향으로 가는 첫 번째 계단이다. 이 실험실에서 시작된 여정이 수술실에 도착할 때, 장기 의학의 역사는 완전히 새로운 장을 열게 될 것이다.
출처 / 참고 데이터
- Engineered tissue offers hope for babies born with missing food pipe section — UCL News
- Lab-grown oesophagus restores pigs ability to swallow — Nature
- GOSH Charity-funded team engineers first lab-grown oesophagus — GOSH Charity
- Esophageal Atresia - Birth Defects — CDC
- Tissue Engineering Market Size To Reach $43.13Bn By 2030 — Grand View Research
- Engineered tissue offers hope for children born with missing esophagus — Medical Xpress
- Adult outcomes following neonatal oesophageal atresia — Nature Pediatric Research